“感度・特異度”だけで満足していませんか?〜HINTS試験に学ぶ、診断研究の正しい読み方〜
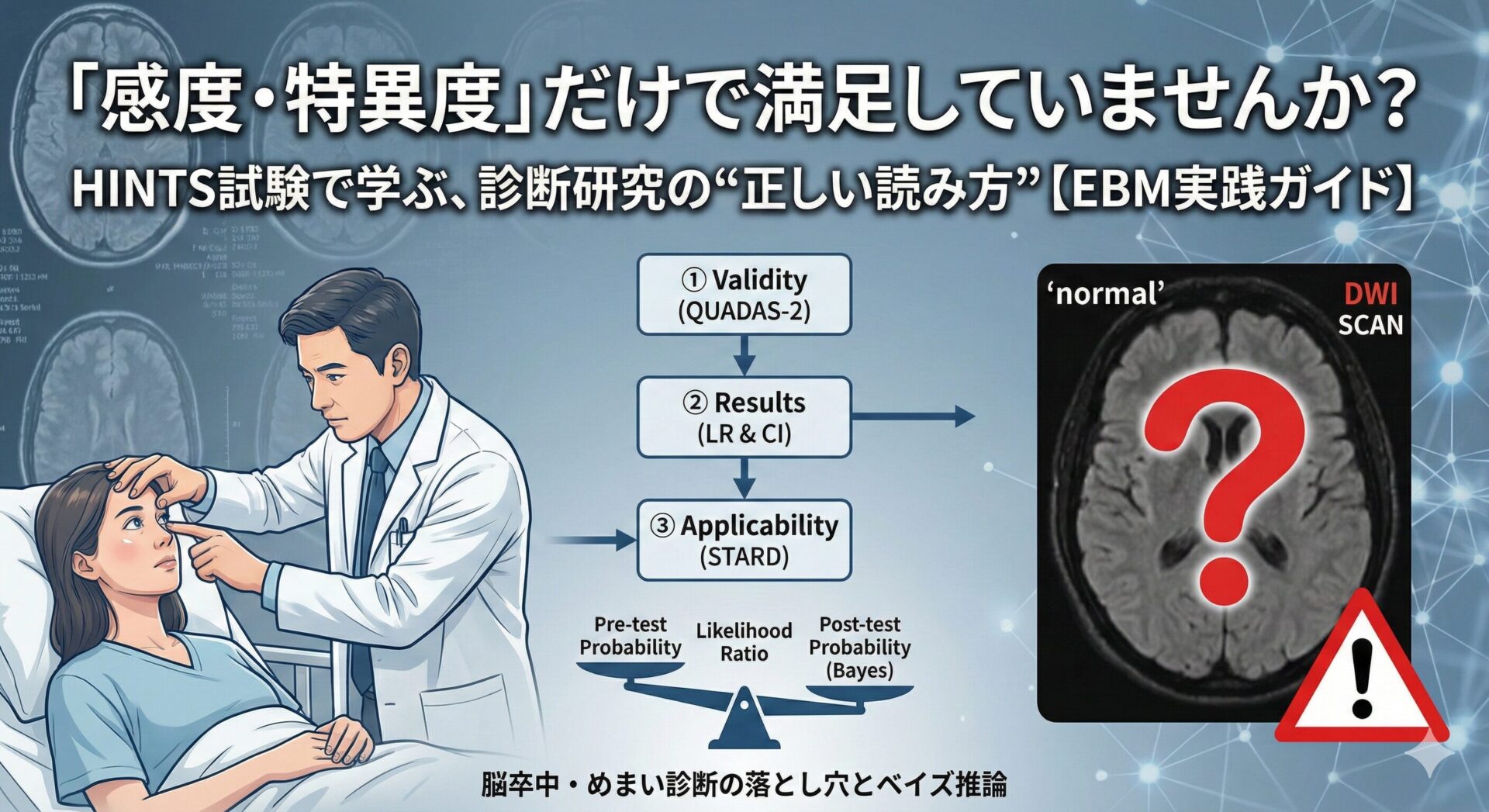
はじめに:MRIが陰性なら安心か?
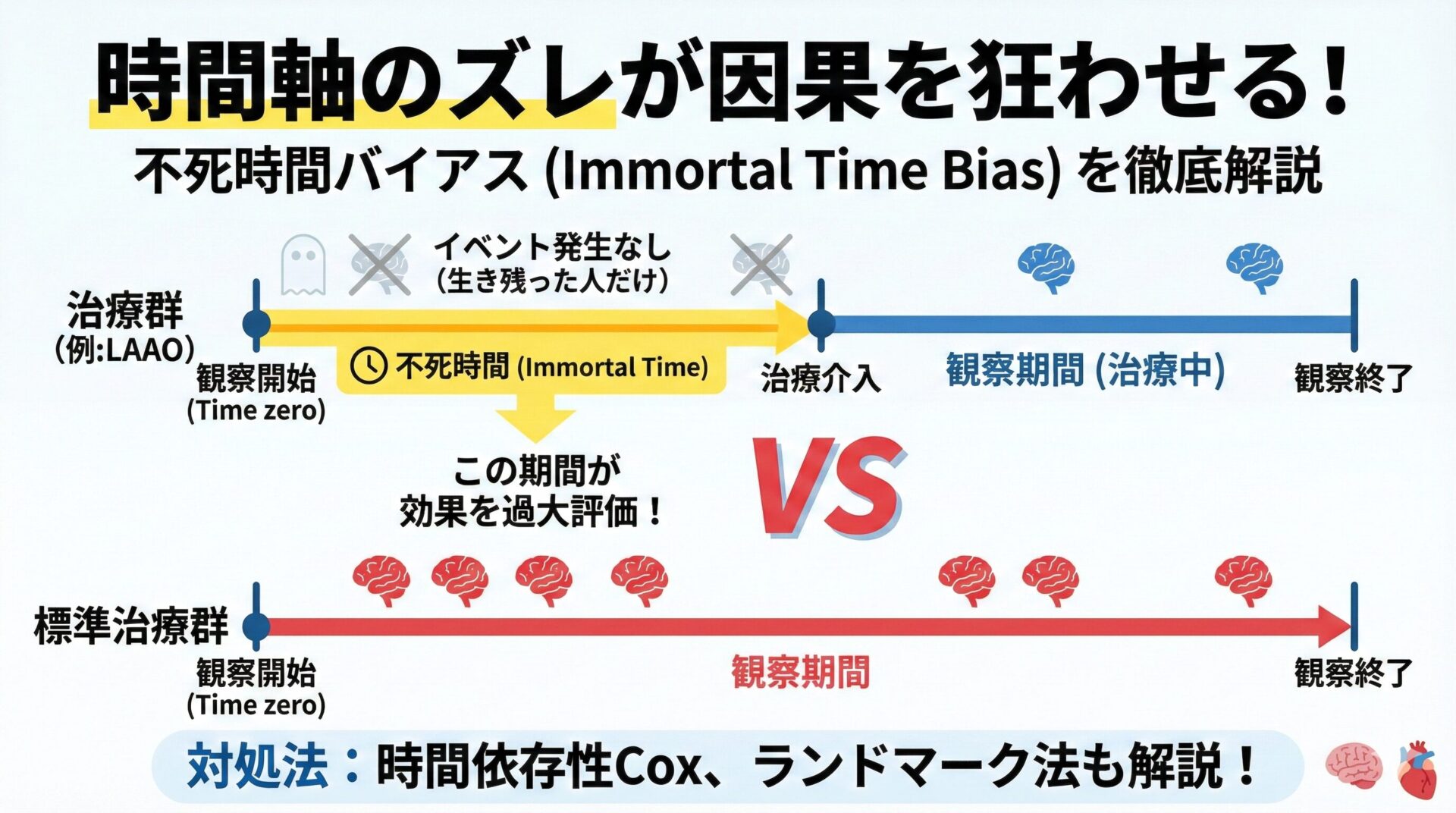
脳神経内科医や脳神経外科医、救急医にとって、急性めまい(Acute Vestibular Syndrome: AVS)ほど神経を使う主訴はありません。
頭部MRI(特にDWI)がきれいだから帰宅とした翌日に脳梗塞が完成していた、という苦い経験談は枚挙にいとまがありません。特に、発症24時間以内の後方循環系梗塞における頭部MRIの偽陰性は無視できない頻度です。
そんな時、頼りになるのが身体所見ですが、新しい検査手技や身体所見の有用性を説く論文に出会った時、先生方はどう読んでいますか?感度100%という数字だけを見て飛びつくのは危険です。
本記事の目的は、HINTS試験そのものの解説ではありません。
HINTS試験を例題として使い、あらゆる診断精度研究に応用できる読み方の型を習得することです。
今回は、バイアス評価ツール(QUADAS-2)と、報告ガイドライン(STARD 2015)の視点を取り入れ、診断研究に関する論文を批判的吟味するスキルを共有します。
以下の順に読み進めていくとよいでしょう。
① 研究デザインを疑う
② 結果を読む
③ ベイズ推論で臨床に適用する
④ あなたの現場で使えるか?
① 研究デザインを疑う
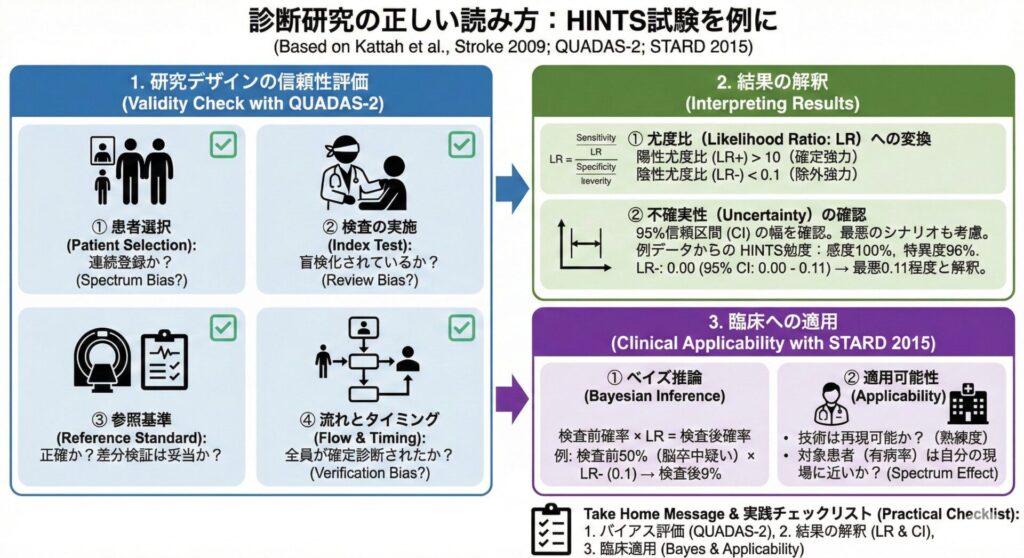
論文の結果を見る前に、まずは方法を見てこの研究は信じるに値するか?を評価します。
ここで役立つ最強のチェックリストがQUADAS-2です。
主に以下の4領域でバイアスをチェックします。
1. 患者選択:スペクトラム・バイアス
- Check: 患者は連続登録されたか?それとも、恣意的な便宜的抽出か?
- HINTS論文の場合: 三次救急の脳卒中センターを受診した連続症例です。しかし、脳卒中センターに来る患者は最初から重症度や脳卒中の確率(有病率)が高い集団です。プライマリ・ケアのセッティングとは患者層が異なるため、感度が過大評価されている可能性があります(=スペクトラム・バイアス)。
2. 検査の実施:盲検化
- Check: Test(ここでは、HINTS)を行う医師は、参照基準(ここでは、MRIの結果)を知らずに評価したか?
- HINTS論文の場合: 検査者はMRI前に評価を行っています。もしMRIの結果を知った後で診察していれば、脳梗塞があるはずだという先入観で所見を取ってしまい、精度が不当に高くなります(=診断的レビュー・バイアス の回避)。
3. 参照基準:差分検証
- Check: 参照基準(正解とする検査)は、病変を正しく分類できるか?全員に同じ基準が適用されたか?
- HINTS論文の場合: ここが重要です。初期MRI-DWIは偽陰性がありうるという前提のため、初期MRI陰性例にはフォローアップのMRIや臨床経過、温度眼振検査などを行い、最終診断を確定させています。
このように状況に応じて追加の基準を用いることを差分検証と呼びます。
偽陰性を拾うために必須の手続きである一方、参照基準が複数になること自体がバイアス源(定義の一貫性など)にもなり得るため、注意が必要です(=差分検証バイアス)。
4. 流れとタイミング:検証バイアス
- Check: 全員が参照基準による確定診断を受けたか?
- HINTS論文の場合: 全例にMRIが行われています。HINTSで陽性の人だけMRIを撮り、陰性の人は帰宅させたというデザインだと、陰性の人の中にある脳梗塞(偽陰性)が永遠に見つからず、感度が高く算出されてしまいます(=検証バイアス )。
② 結果を読む
バイアスチェックを通過したら、いよいよ結果の数字を見ます。
診断研究の結果は「2×2表(分割表)」から始まります。
1. 感度・特異度から“尤度比”へ
感度・特異度は、病気の有無が決まっている集団での検査の確率ですが、臨床で知りたいのは、検査結果が出た後の、病気の確率です。
その変換に使うのが尤度比(Likelihood Ratio: LR)です。
- 陽性尤度比 (LR+) = 感度 / (1 – 特異度)
- 目安:10以上あれば確定診断に強力に働く。
- 陰性尤度比 (LR-) = (1 – 感度) / 特異度
- 目安:0.1以下あれば除外診断に強力に働く。
2. 不確実性を見る:95%信頼区間(CI)
HINTS試験の結果を見てみましょう。
- 感度 100%, 特異度 96%
- LR+ : 25.0
- LR- : 0.00 (95% CI: 0.00 – 0.11)
数字だけ見ると完璧に見えますが、必ず95%信頼区間(CI)を確認してください。
本研究のLR-は点推定値では0.00ですが、CI上限は0.11です。
統計的な誤差を含めると、最悪の場合、LR-は0.11程度かもしれないと解釈するのが、正しい読み方です。
③ ベイズ推論で臨床に適用する
得られたLRを使って、目の前の患者さんの確率を計算します(=ベイズの定理)。
ここでは、安全域を見積もるため、LR-のCI上限である0.11を0.1に丸めて計算してみましょう。
シナリオ
60歳男性、高血圧、糖尿病あり。今朝からの激しい回転性めまい・嘔吐。頭痛なし。麻痺なし
先生の直感(病歴からの検査前確率)が脳卒中の確率は 50% (0.5)だとします。
HINTSが末梢性パターン(陰性)だった場合
LR- (0.1) を使って検査後確率を推測します。
- オッズ比の計算:検査前オッズ (0.5/0.5 = 1) × LR- (0.1) = 検査後オッズ 0.1
- 確率への変換:0.1 / (1 + 0.1) ≒ 0.09 (9%)
検査前50%だった脳卒中の確率は、HINTSが完全に末梢性を示唆すれば、約9%まで下がります(LR-が0.00なら理論上は0%ですが、CI上限を使うことで過信を防げます)。
9%も残るならMRIを撮ろうとなるか、9%なら帰宅可能とするか。それは臨床状況次第ですが、少なくともLRを使えば、検査結果が確率をどう動かすかを定量化できる点が重要です。
④ あなたの現場で使えるか?
最後に、最も重要な適用可能性です。ここでSTARD 2015(報告ガイドライン)の視点が役立ちます。
論文に、自分の現場で再現できるだけの情報が書かれているか?を確認するのです。
- 誰がやったのか?(検者の熟練度)
HINTS論文の検査者は神経眼科医です。
Head Impulse Testの急速な眼球運動を目視で判定するのは習熟を要します。論文通りに再現できる技術が自分にあるか?
技術への依存度が高い検査であることに注意が必要です。 - 対象患者とセッティング(スペクトラム効果と予測値)
感度・特異度は理想的には検査固有の性質とされますが、実際には患者のスペクトラム(重症度や併存疾患)によって変動します(=スペクトラム効果)。
また、陽性適中率(PPV)・陰性適中率(NPV)は有病率に強く依存します。
脳卒中センター(高有病率)で得られたPPVは、一般のめまい外来(低有病率)ではそのまま通用しません。
STARDのフロー図を見て、どのような患者募集(連続登録か否か)が行われたかを確認し、自分の患者層とのズレを補正して考える必要があります。
Take Home Message & 実践チェックリスト
診断研究を読むときは、HINTSはすごい診断能の検査で終わらせず、なぜこの研究は信頼できるのかを以下のチェックリストで点検してください。
診断研究論文の読解用チェックリスト
(1) バイアス評価 (QUADAS-2)
- □ 患者選択: 連続登録か?(スペクトラム・バイアスはないか?)
- □ Index Test: 結果を知らずに行ったか?(盲検化・レビューバイアス)
- □ 参照基準: 正確に分類できるか?(差分検証の妥当性)
- □ フロー: 全員が参照基準で確定診断されたか?(検証バイアス)
(2) 結果の解釈 (Results)
- □ LRの確認: LR+ >10, LR- <0.1 を目安にする。
- □ CIの確認: 信頼区間の幅(最悪のシナリオ)を確認する。
(3) 臨床適用 (Application)
- □ ベイズ推論: [検査前オッズ × LR = 検査後オッズ] で確率を計算する。
- □ 適用可能性: 技術は再現可能か? 対象患者(有病率)は自分の現場に近いか?
参考文献
- Kattah JC, Talkad AV, Wang DZ, Hsieh YH, Newman-Toker DE. HINTS to diagnose stroke in the acute vestibular syndrome: three-step bedside oculomotor examination more sensitive than early MRI diffusion-weighted imaging. Stroke. 2009;40(11):3504-3510. doi:10.1161/STROKEAHA.109.551234
PUBMED: https://pubmed.ncbi.nlm.nih.gov/19762709/ - Whiting PF, Rutjes AW, Westwood ME, et al. QUADAS-2: a revised tool for the quality assessment of diagnostic accuracy studies. Ann Intern Med. 2011;155(8):529-536. doi:10.7326/0003-4819-155-8-201110180-00009
PUBMED: https://pubmed.ncbi.nlm.nih.gov/22007046/ - Bossuyt PM, Reitsma JB, Bruns DE, et al. STARD 2015: an updated list of essential items for reporting diagnostic accuracy studies. BMJ. 2015;351:h5527. Published 2015 Oct 28. doi:10.1136/bmj.h5527
PUBMED: https://pubmed.ncbi.nlm.nih.gov/26511519/