臨床試験の単純比較はNG!〜DOACの大規模RCTから学ぶ試験横断比較〜
はじめに
外来や病棟で、研修医の先生や他科の先生からこんなふうに聞かれたことはないでしょうか。
「先生、DOACっていろいろありますけど、結局どれが一番いい薬なんですか?」
非弁膜症性心房細動(NVAF)の脳卒中予防では、複数の直接作用型経口抗凝固薬(DOAC)が使える時代になりました。
その中で、一番安全で、かつ効果が高いのはどれか?という疑問は、多くの医療者が一度は抱くものだと思います。
今回は、DOACの代表的な臨床試験を引き合いに出しながら、直接比較(Head-to-head)試験がない状況で、異なる試験の数字を横断的に比べてはいけないという、疫学・統計学の重要な原則について解説します。
DOACの金字塔:ARISTOTLE試験
まずは、アピキサバン(商品名:エリキュース®)の有効性と安全性をワルファリンと比較した、有名なランダム化比較試験(RCT)であるARISTOTLE試験を簡単に振り返ります。
【PICO】
- P: 脳卒中リスク因子を有する非弁膜症性心房細動患者
- I: アピキサバン 5 mg 1日2回投与
- C: ワルファリン投与(目標PT-INR 2.0–3.0)
- O: 脳卒中または全身性塞栓症の発生(有効性)、大出血の発生(安全性)
【結果】
アピキサバンはワルファリンと比較して、脳卒中・全身性塞栓症のリスクを有意に減らし、大出血のリスクも有意に減少させました。
なぜ試験同士を比較してはいけないのか
単純比較の罠
ARISTOTLE試験だけを見ると、アピキサバンは大出血リスクを大きく減らしている。ならば最も優れたDOACではないか?と言いたくなります。
しかし、ここに大きな落とし穴があります。
リバーロキサバンとワルファリンを比較したROCKET AF試験の結果と単純に並べて、アピキサバンの方が安全だ、と結論づけるのは不適切です。
ROCKET AF試験では大出血全体ではワルファリンとの有意差はありませんでしたが、頭蓋内出血や致死的出血は有意に少ないという結果でした。
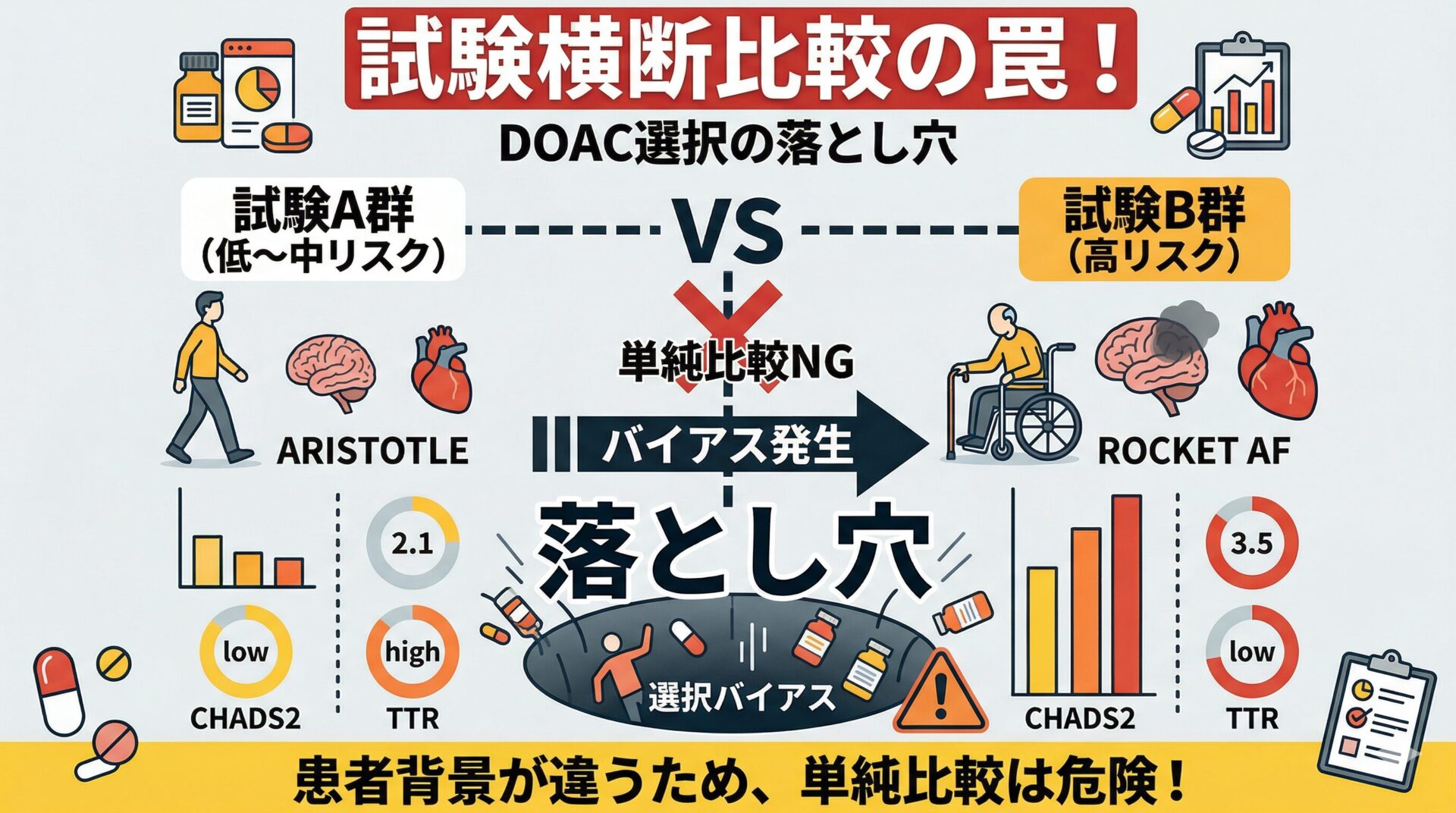
さらに重要なのは、ROCKET AF試験の集団はARISTOTLEよりもはるかに高リスクだったことです。つまり、異なる背景をもつ集団の結果を横に並べただけでは薬剤そのものの優劣は判断できません。
これはアピキサバンとリバーロキサバンの2剤だけの話ではなく、DOAC試験全体に共通する落とし穴です。
以下のDOAC主要4試験の比較表をご覧ください。
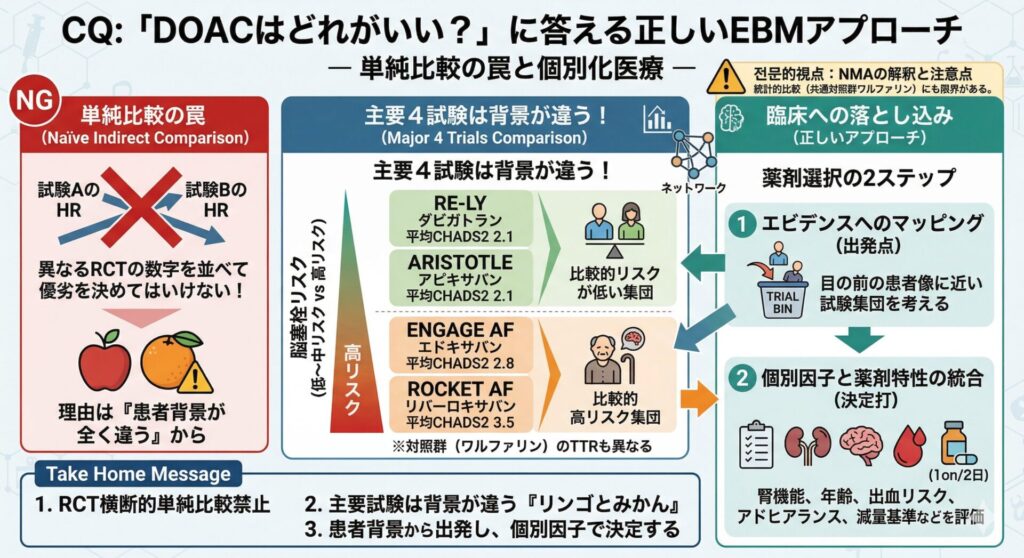
| 試験名 | 薬剤名 | CHADS2スコア(平均) | ワルファリン群のTTR | 試験集団の特徴 |
| RE-LY | ダビガトラン | 2.1点 | 約64% | 比較的低〜中等度のリスク集団 |
| ARISTOTLE | アピキサバン | 2.1点 | 約62% | 比較的低〜中等度のリスク集団 |
| ENGAGE AF-TIMI 48 | エドキサバン | 2.8点 | 約68% | 中〜高リスク集団 |
| ROCKET AF | リバーロキサバン | 3.5点 | 約55% | 比較的高リスク集団 |
※TTR (Time in Therapeutic Range): PT-INRが治療域に収まっていた時間の割合
一目瞭然ですね。ROCKET AF試験やENGAGE AF-TIMI 48試験に参加している患者さんの方がそもそも脳梗塞発症リスクが高く、併存疾患も多い集団なのです。
対照群であるワルファリンのコントロール状況(TTR)も試験ごとに異なります。
全く異なる集団で行われた試験を直接比較することは、RCT最大の強みであるランダム化の恩恵を無にし、強烈な選択バイアスを生み出してしまいます。
専門的視点:NMA(ネットワークメタアナリシス)の解釈と注意点
共通の対照群(=ワルファリン)を介して統計的に比較する、ネットワークメタアナリシス(NMA)なら良いのでは?と考える先生もいるでしょう。
確かに、NMAはHead-to-head試験が不在の状況下において、非常に有用な補助手段です。しかし、NMAは推移性(Transitivity:試験間で結果に影響を与える患者背景が十分に似ていること)という前提に依存しています。
DOACの主要試験群では、上記の通りCHADS2スコアやTTRだけでなく、試験デザインやアスピリンの併用率なども異なります。
既存のNMA論文でも、これらの重要な効果修飾因子(患者背景やTTRの差など)を完全には調整しきれないことが限界として繰り返し指摘されており、その解釈には慎重な姿勢が求められます。
臨床への落とし込み:では、どう選ぶのか?
薬剤選択に迷ったとき、異なるRCTのハザード比を並べて優劣を決めるべきではありません。
実際の臨床現場におけるDOAC選択は、以下のステップで思考を整理するとスムーズです。
1. エビデンスへのマッピング(出発点)
まずは、目の前の患者さんがどの臨床試験の患者集団に近いかを考えます。
(例:高齢で脳卒中既往があるハイリスク患者ならROCKET AFやENGAGE AF寄り、比較的低リスクならARISTOTLEやRE-LY寄り)。
2. 患者個別因子と薬剤特性の統合(決定打)
そのうえで、腎機能、年齢、体重、出血リスク、服薬アドヒアランス(1日1回か2回か)、併用薬、減量基準などを踏まえて最終的な薬剤を選ぶ。
この順番で考えると、DOAC選択はかなり整理しやすくなります。
数字の良し悪しで薬を決めるのではなく、エビデンスを出発点としつつ、目の前の患者の個別要因を統合することこそが、真のEBM(Evidence-Based Medicine)と言えます。
Take Home Message
- 異なるRCTのハザード比を横断的に比較して、薬剤の優劣を決めてはいけない。
- DOACの主要試験は、対象患者のCHADS2スコアやTTRが大きく異なっており、単純には比較できない“リンゴとみかん”である。
- 処方の際は、目の前の患者像がどの試験に近いかを出発点とし、腎機能や服薬アドヒアランス等の個別因子を統合して薬剤を選択する。
日々の診療や抄読会でついついこっちの薬の方が数字が良いと言いそうになった時は、ぜひこのリンゴとみかんの原則を思い出してみてください。
参考文献
- Granger CB, Alexander JH, McMurray JJ, et al. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2011;365(11):981-992.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/21870978/ - Patel MR, Mahaffey KW, Garg J, et al. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med. 2011;365(10):883-891.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/21830957/ - Iyer V, Wang DY, Reiffel JA. Cross-trial comparisons: a source of confusion, use, or both in the management of patients with atrial fibrillation?. Am Heart J. 2013;165(6):882-892.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/23708158/ - Camm AJ, Fox KAA, Peterson E. Challenges in comparing the non-vitamin K antagonist oral anticoagulants for atrial fibrillation-related stroke prevention. Europace. 2018;20(1):1-11.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/29040518/