高齢者てんかんにおける酵素誘導性抗てんかん発作薬と心血管リスク 〜JAMA Neurology 2024の論文から考える〜
はじめに
高齢者てんかんの診療において、薬剤選択は常にジレンマの連続です。
発作抑制が最優先ですが、併存症やポリファーマシー(多剤併用)の問題、そして長期的な副作用リスクを天秤にかける必要があります。
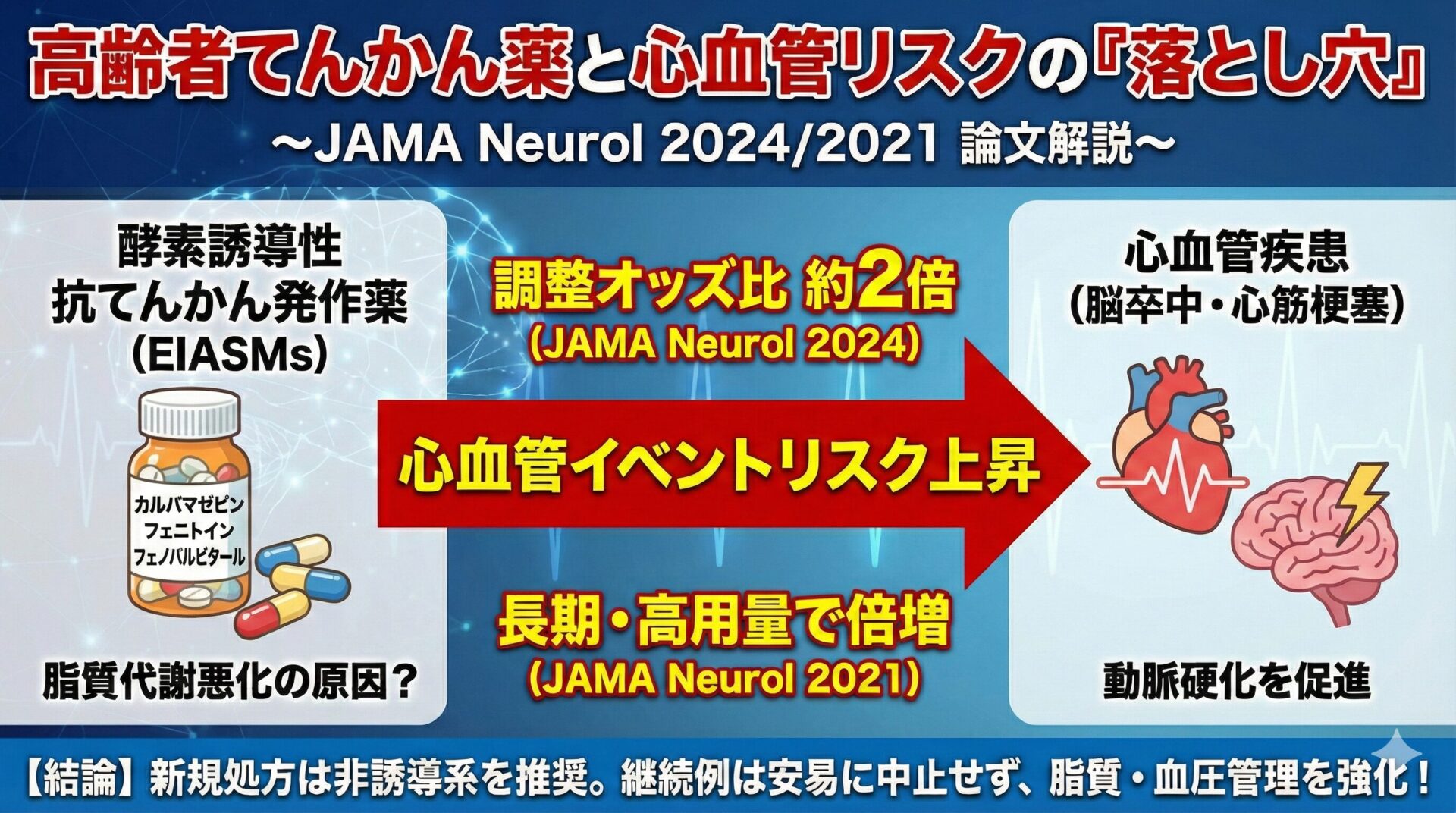
特に、カルバマゼピンやフェニトインといった、酵素誘導能を持つ抗てんかん発作薬(Enzyme-Inducing Antiseizure Medications: EIASMs)が、動脈硬化を促進して心血管イベントを増やすのではないか?という懸念は、近年のホットトピックスです。
今回は、このテーマに新たな視点を与えた2024年の最新論文(Li, et al.)とその基礎となる2021年の重要論文(Josephson, et al.)を整理し、私たち臨床医が明日からどう動くべきか、その落とし所について解説します。
今回のメイン論文
JAMA Neurology 2024 (Li, et al.)
まずは、最新の研究紹介です。この研究は、カナダの高齢者コホートを用いた前向き研究で、てんかんそのもののリスクとEIASMsによる媒介効果を解析しています。
研究のPICO
- P (Patient): Canadian Longitudinal Study on Aging (CLSA) に登録された45~85歳の地域住民コホート(ベースラインで心血管疾患なし)。
- E (Exposure): 生涯てんかん歴あり(+EIASMsの使用状況や心血管リスク因子を媒介因子として評価)。
- C (Comparison): てんかん歴のない参加者。
- O (Outcome): 6年間の追跡における新規心血管イベント(心筋梗塞、脳卒中、TIAなど)。
結果の概要:リスクの正体は薬か?
解析の結果、てんかん歴のある群は、ない群と比較して新規心血管イベント(CVE)の調整オッズ比が約2倍(OR 2.20)と高値でした。
ここで注目すべきは、なぜリスクが高いのかという点です。
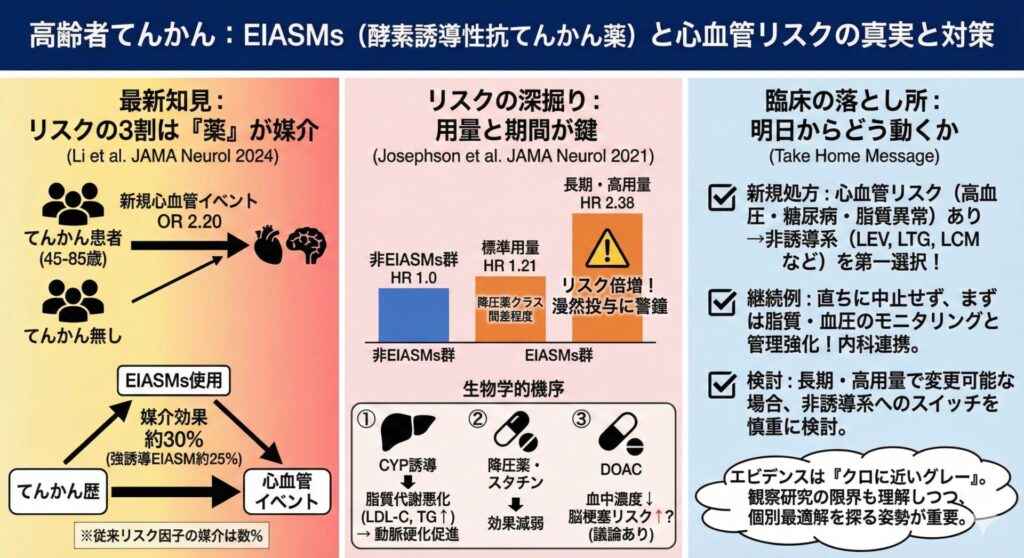
解析の結果、てんかん歴と新規CVEの関連のうち、約3割がEIASMの使用によって媒介されていると推定されました。
- 強いEIASM(CBZ, PHT, PB等): 約25%を媒介
- 弱いEIASM: 約4%を媒介
一方で、Framinghamスコアなどの従来型リスク因子の媒介効果は数%程度にとどまりました。つまり、てんかん患者のCVDリスクが高いのは、従来のリスク因子(血圧や糖尿病)が悪いからというよりは、EIASMsを飲んでいること自体の影響が大きいのではないかという仮説が浮かび上がります。
薬剤リスクの深掘り
JAMA Neurology 2021 (Josephson, et al.)
では、具体的にEIASMsはどの程度リスクを上げるのでしょうか?
これについては、Li論文の前提ともなっている、2021年の英国大規模データ(Josephson et al.)がより直接的な答えを持っています。
こちらは英国の診療記録(CALIBER)を用いたコホート研究で、EIASMs使用者 vs 非EIASMs使用者を直接比較しています。
結果のハイライト:用量と期間が鍵
- EIASMs群は、非EIASMs群と比較して、心血管疾患(虚血性心疾患、脳卒中)のハザード比 (HR) が 1.21 (95% CI 1.06–1.39) でした。
- さらに重要なのは、長期・高用量(相対的な一日平均維持投与量が2以上)の場合、HRは 2.38 まで上昇したという点です。
臨床的見解
この数字をどう捉えるべきでしょうか?
標準的な用量におけるHR 1.21は、疫学的な感覚で言えば降圧薬のクラス間(種類による)の差と同程度のインパクトであり、直ちに毒薬扱いするほどではありません。
しかし、長期・高用量ではリスクが倍増する(HR > 2.0)というデータは、漫然と処方を続けることへの強い警鐘と言えます。
なぜリスクが上がるのか?
(生物学的機序と相互作用)
EIASMsによる心血管リスク上昇には、もっともらしい生物学的機序が存在します。
- 脂質代謝への悪影響:CYP酵素誘導により、総コレステロール、LDLコレステロール、トリグリセリド、ホモシステインなどを上昇させることが複数の研究で示されています。これが動脈硬化の直接的なドライバーとなります。
- 併用薬の効果減弱(相互作用):降圧薬やスタチンなどの代謝を促進し、それらの効果を減弱させる可能性が指摘されています。
- DOAC(直接作用型経口抗凝固薬)との関係:理論的には、EIASMsがDOACの血中濃度を下げ、脳梗塞リスクを増やす懸念があります。ただし、2024-2025年の大規模コホート研究では、EIASMs併用による脳卒中・血栓イベントの有意な増加は確認されなかったという報告もあり、臨床的な意義については議論が続いています。とはいえ、添付文書上は注意が必要な組み合わせであることに変わりはなく、個別の判断が求められます。
批判的吟味:観察研究の限界
注意点として、これらはあくまで観察研究であることは忘れてはいけません。
- 未測定交絡:多変量解析で補正しても、EIASMsが選ばれるような患者背景(難治例、古い治療歴など)や測定されていないライフスタイルの影響は完全には排除できません。
しかし、脂質代謝への悪影響という生物学的裏付けがある以上、この関連性はクロに近いグレーとして臨床判断に組み込むのが賢明です。
日常診療へのTake Home Message
エビデンスと限界を踏まえ、現場での落とし所を提案します。
- 新規処方の患者さんには、これから抗てんかん薬を開始する高齢者、特に心血管リスク(高血圧、糖尿病、脂質異常症)を持つ患者さんに対しては、非酵素誘導系(レベチラセタム、ラモトリギン、ラコサミド等)を第一選択とすることを強く推奨します。これは近年のガイドラインの潮流とも合致します。
- 既にEIASMsを服用中の患者さんには、心血管リスクがあるからといって、発作が抑制されている薬剤を直ちに変更する必要はありません。安易な変更で発作再発を招くリスクの方が高い場合も多々あります。
その代わり、以下の管理を徹底してください。
- モニタリング強化: 定期的な脂質プロファイル(LDL-C)、血圧のチェックを行う。
- リスク因子の治療: 脂質異常等があれば、スタチン導入などを内科と連携して行う。
- 変更の検討: もし長期・高用量であり、かつ変更しても発作抑制が維持できそうなケースであれば、非誘導系へのスイッチを慎重に検討する価値があります。
まとめ
- てんかん患者のCVDリスク上昇の約3割は、EIASMs(特に強誘導薬)の使用によって媒介されている可能性がある (JAMA Neurol 2024 Li et al.)。
- EIASMsの使用はCVDリスク上昇(HR 1.21)と関連し、長期高用量ではリスクが倍増する (JAMA Neurol 2021 Josephson et al.)。
- DOACとの併用は理論的懸念があるが、近年のコホートでは臨床イベントの明確な増加は示されていない。
- 新規なら非誘導系を推奨。継続例なら、直ちに中止せず脂質・血圧管理を強化し、ハイリスク例では薬剤変更も選択肢に入れる。
参考文献
- Li J, Shlobin NA, Thijs RD, et al. Antiseizure Medications and Cardiovascular Events in Older People With Epilepsy in the Canadian Longitudinal Study on Aging. JAMA Neurol. 2024;81(11):1178-1186.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/39804367/ - Josephson CB, Wiebe S, Delgado-Garcia G, et al. Association of Enzyme-Inducing Antiseizure Drug Use With Long-term Cardiovascular Disease. JAMA Neurol. 2021;78(11):1367-1374.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/34605857/