てんかん重積状態の早期追加治療:ラコサミド vs レベチラセタム 〜日本のDPCデータベース研究から考える〜
はじめに
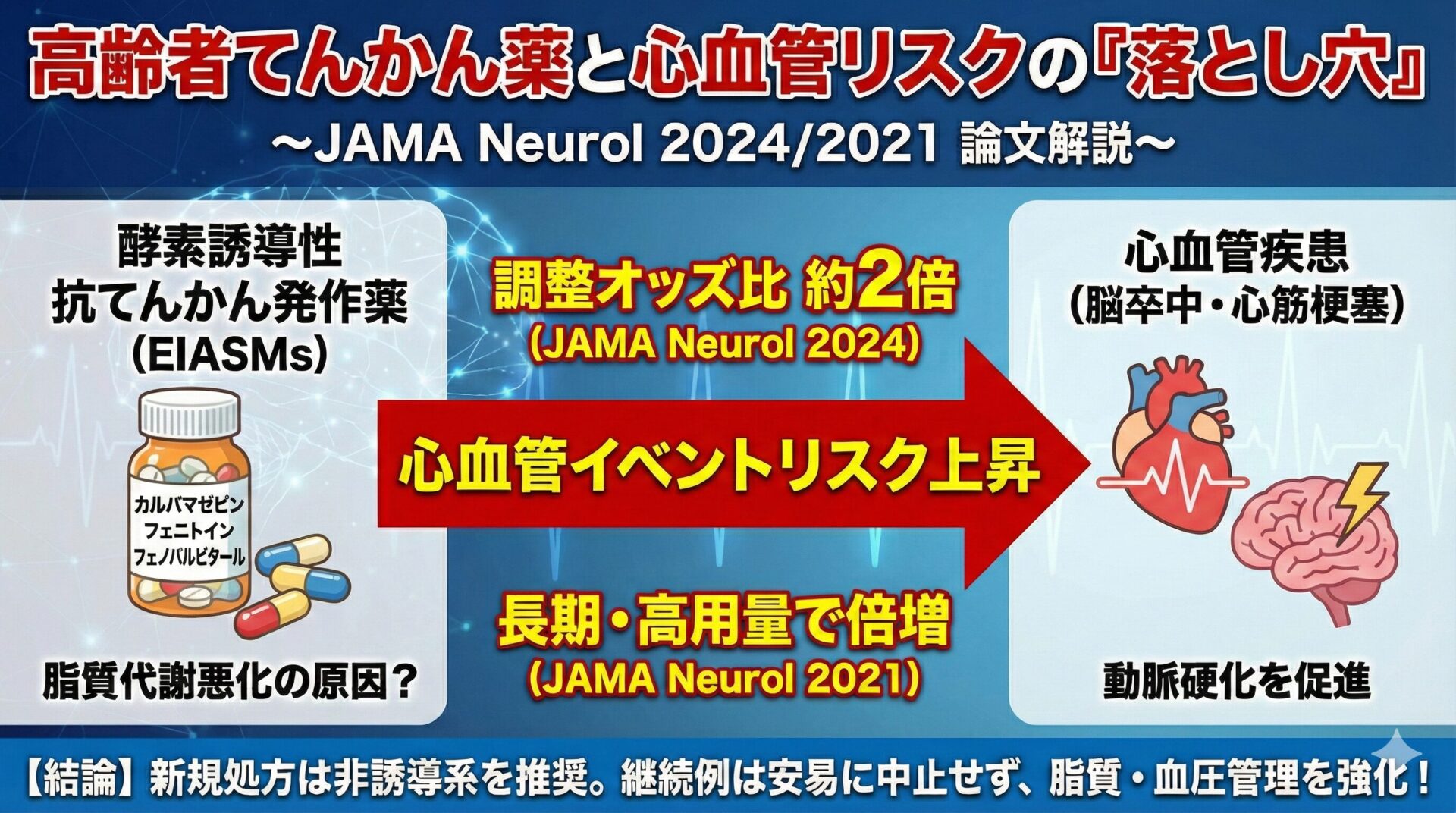
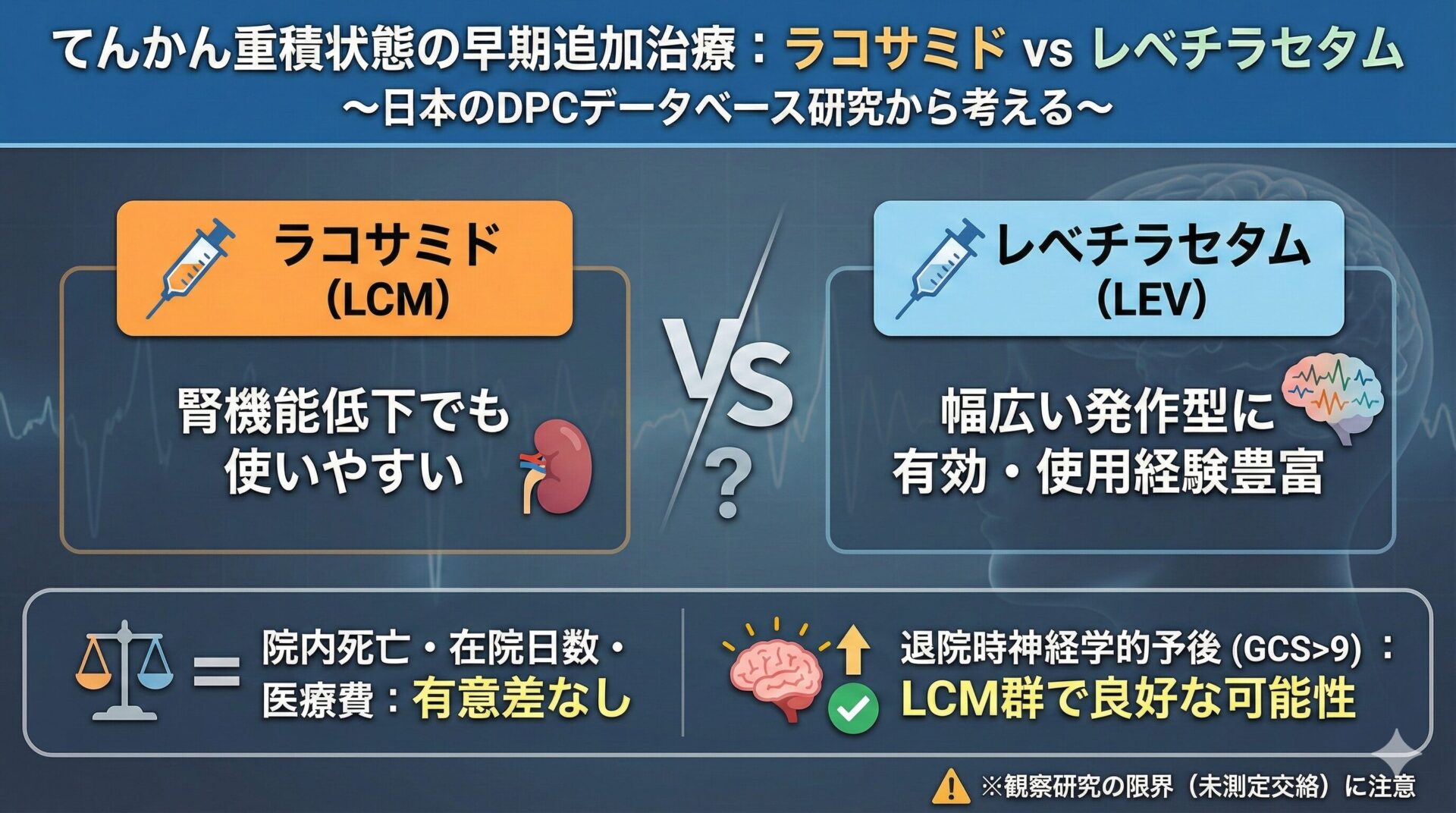
脳神経内科の診療において、てんかん重積状態は迅速な対応が求められる神経救急疾患です。初期治療としてのベンゾジアゼピンに続く追加治療として、本邦では静注用のレベチラセタム(LEV)やラコサミド(LCM)が広く用いられています。
しかし、日本の実臨床データに基づいて両者を直接比較した報告は限られていました。今回、日本全国の急性期病院をカバーするDPCデータベースを用いた後ろ向きコホート研究が報告され、てんかん重積状態の早期追加治療としてのLCMとLEVの院内アウトカムが比較されています。
研修医・専攻医の先生方や、非専門医の先生方にも分かりやすく研究デザインの読み解き方と臨床への応用について解説します。
紹介する論文のPICO
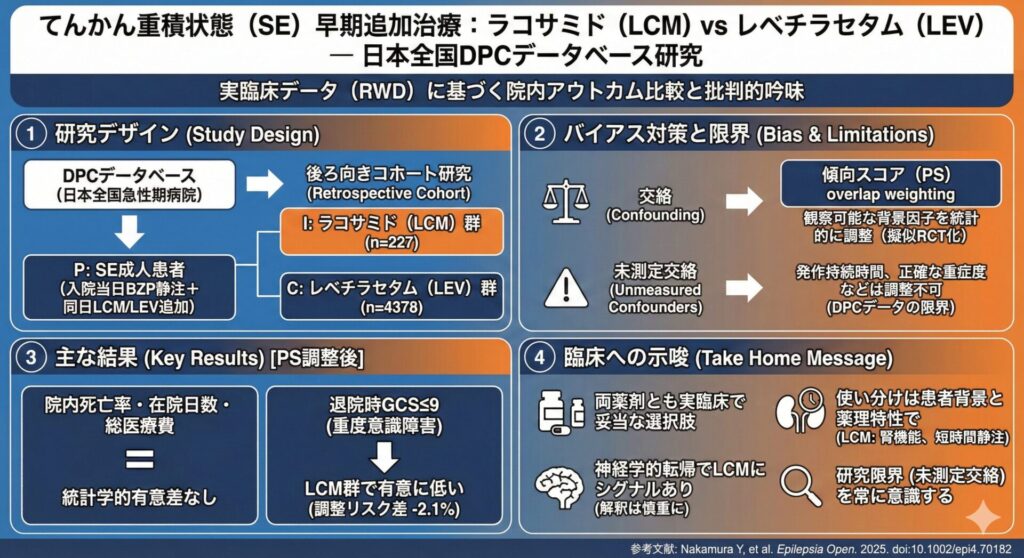
P (Patients): 日本のDPCデータベースに登録された、てんかん重積状態で入院し、入院当日にジアゼパムまたはロラゼパム静注を受けたうえで、同日にラコサミドまたはレベチラセタムの静脈内投与を追加された成人患者(2019年4月〜2023年3月退院例)
I (Intervention): ラコサミド静脈内投与(入院当日の早期追加治療)
C (Comparison): レベチラセタム静脈内投与(入院当日の早期追加治療)
O (Outcome): 院内死亡率、在院日数、総医療費、および退院時のGlasgow Coma Scale(GCS)スコア≤9の割合
研究デザインの解説と批判的吟味
この研究は、日本の全国的な入院患者データベース(DPCデータベース)を用いた、後ろ向きコホート研究です。
リアルワールドデータの強み
DPCのような大規模データベース研究は、いわゆるリアルワールドデータを用いた研究であり、ランダム化比較試験(RCT)とは異なる強みがあります。
- 外的妥当性(Generalizability): RCTのように厳格な選択基準・除外基準がなく、日常診療(実臨床)で遭遇する多様な患者背景(高齢者、併存疾患の多い患者など)を反映しているため、研究結果を実臨床に適用しやすい可能性があります。
- 大規模なサンプルサイズ: 本研究では約4600例と、多くの症例を解析できています。
後ろ向き研究の限界:交絡との戦い
一方で、この研究はRCTではないため、なぜ医師はLCMを選び、なぜLEVを選んだのか という治療選択そのものにバイアスが潜んでいます。これを交絡と呼びます。
例えば、腎機能が悪い患者には、腎排泄型のLEVを避けて肝代謝型のLCMが選択されやすかった、といった可能性(=適応による交絡)が考えられます。もしLCM群とLEV群で、投与開始前の患者背景(重症度、併存疾患、腎機能など)が異なっていれば、アウトカムの差が薬剤の効果によるものか、元の患者背景の差によるものか、区別がつかなくなります。
統計手法による交絡の調整
本研究では、交絡を軽減するために、傾向スコアを用いたoverlap weighting という手法が用いられています。
補足:傾向スコア (PS) とは?
傾向スコアとは、年齢、性別、併存疾患、重症度など観察できる共変量に基づいて、各患者がLCMを投与されやすさを0〜1の連続値で表したものです。
傾向スコアを用いた交絡調整には、マッチング、層別解析、逆確率重み付けなど様々な手法があります。本研究で用いられた overlap weighting もその一種です。
overlap weightingでは、このスコアに応じて各患者に重み付けを行うことで、両薬剤のいずれを選択してもおかしくない(=PSが中間的な)患者集団を解析上で強調し、背景因子のバランスがとれた“仮想的な比較集団”を構成します。
これにより、“観察された”交絡因子については、RCTに近い状況を統計学的に再現しようと試みています。
批判的吟味:残存するバイアス
ただし、PSによる調整は万能ではありません。
最大の限界は、未測定の交絡因子は調整できない点です。
DPCデータには、SEの予後に影響しうる重要な臨床情報、例えば、発作の正確な持続時間、発作の正確な分類(けいれん性か非けいれん性か)、初期のベンゾジアゼピン投与量、治療開始までの正確な時間、といった詳細な情報が含まれていません。
これらの測定されていない因子が治療選択とアウトカムの両方に関連していた場合、PSを用いた調整を行ってもその交絡は除去できず、結果が歪んでいる(バイアスが残存している)可能性があります。
研究の結果と臨床的意義
本研究では、DPCデータベースから抽出された4605例(LCM 227例、LEV 4378例)のSE症例が解析対象となりました。(LCM群が著しく少ない点も、実臨床を反映している可能性があります。)
傾向スコアoverlap weighting後の解析では、院内死亡率、在院日数、総医療費について、LCM群とLEV群の間に統計学的に有意な差は認められませんでした。
一方で、退院時GCSスコア≤9(重度の意識障害が残存していると考えられる状態)の患者割合は、LCM群でLEV群よりも有意に低いという結果が示されています(調整済みリスク差 -2.1%、95%信頼区間 -3.3〜-0.9)。
この結果をどう解釈すべきでしょうか?
この大規模な実臨床データからは、入院当日の早期追加治療としてLCMを選択した場合、院内死亡や在院日数といったマクロなアウトカムに大きな違いはないものの、退院時の神経学的状態がわずかに良好である可能性が示唆される、と解釈できます。
ただし、これはあくまで後ろ向き観察研究の結果です。前述の通り、重症度や発作持続時間などの未測定交絡が残存している可能性は否定できません。
LCMがLEVより明確に優れていると断定するには、今後の前向き研究(理想的にはRCT)による検証が必要です。
Take Home Message
今回の研究結果は、我々臨床医にとってどのような示唆を与えるでしょうか。
- 両薬剤とも合理的な選択肢である:
ベンゾジアゼピン投与後の早期追加治療として、LCMもLEVも引き続き実臨床における妥当な選択肢であると考えられます。 - マクロな予後は同等、神経学的転帰はLCMに期待か?:
院内死亡や在院日数といった主要なアウトカムは両群で同等でした。一方で、退院時GCS≤9の割合がLCM群で低かったという結果は臨床的に興味深い点です。ただし、これはRCTではないためこの結果のみをもって神経学的予後改善のためにLCMを優先すべきと結論づけるのは早計です。 - 薬剤選択は患者背景と薬理特性に応じて:
どちらでも良いのではなく、両者の薬理学的な特性に基づき、個々の患者背景に応じた使い分けが現実的です。- LCM: 腎機能障害(CKD)や透析患者でも用量調整が比較的容易。比較的短時間(本邦添付文書では30〜60分、海外では15分程度までの報告もあり)での点滴静注が可能です。
- LEV: 幅広い発作型に有効。使用経験が豊富。精神症状の副作用に注意。
- 研究の限界を常に意識する:
本研究は後ろ向き研究であり、未測定の交絡(特に重症度や発作の持続時間)が結果に影響している可能性を常に念頭に置く必要があります。
SEの治療は時間との勝負です。
この研究は私たちが日常的に使用するLCMとLEVという2つの重要な薬剤について、大規模な実臨床データに基づいた貴重な知見を提供してくれました。
参考文献
- Nakamura Y, Aso S, Yasunaga H, et al. In-hospital outcomes of lacosamide versus levetiracetam for early adjunctive treatment of status epilepticus: A Nationwide Japanese retrospective cohort study. Epilepsia Open. Published online November 12, 2025. doi:10.1002/epi4.70182
PUBMED: https://pubmed.ncbi.nlm.nih.gov/41222404/