観察研究の落とし穴:適応による交絡を遠位中血管閉塞に対するEVTに関する臨床研究で学ぶ
はじめに
本記事では、観察研究における交絡の典型例である適応による交絡を扱います。
現場で前方循環の遠位中血管閉塞 (DMVO; Distal Medium Vessel Occlusion) の患者さんを前に、血管内治療 (EVT) を行うべきか、内科的治療でいくべきかと悩む場面は少なくありません。
大血管閉塞(Large Vessel Occlusion;LVO) と異なり、DMVO領域はまだ臨床的に意見の一致が得られていない状態が続いています。そんな中、DMVOに対するEVTの有効性を検証した観察研究の結果を、私たちはどう解釈すればよいでしょうか。
今回は、このDMVOとEVTを扱った具体的な論文を題材に、観察研究の落とし穴であり、最も重要な概念の一つである適応による交絡について学びます。
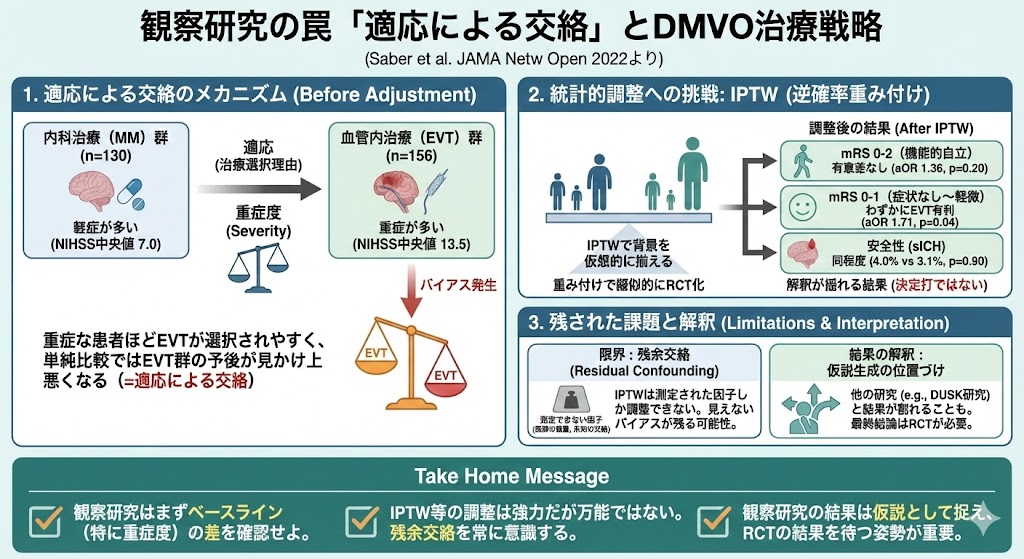
観察研究の落とし穴:適応による交絡とは
私たちが観察研究(コホート研究やレジストリ研究など)を読むとき、常に警戒すべきバイアスがあります。その筆頭が交絡です。
中でも特に厄介なのが、適応による交絡です。
【用語解説】適応による交絡 (Confounding by Indication)
治療(介入)を決定する理由(=適応、例:症状が重いこと)自体が、結果(=予後)とも強く関連しているために生じるバイアス(交絡)のこと。
- (例)重症な患者ほど、積極的な治療(例:新薬、手術)が選ばれやすい。
- しかし、その患者群は元々が重症であるため、治療の有無にかかわらず予後が悪い可能性が高い。
この2群を単純比較すると、積極的治療群の方が予後が悪く見え、あたかもその治療は効果がないあるいは有害であるかのような、誤った結論が導かれてしまう可能性があります。
題材論文のPICOとベースライン(NIHSS差に注目)
この適応による交絡を体感するのに、うってつけの論文がこちらの多施設共同後ろ向きコホート研究 (Saber H, et al. 2022)です。
- P (Patients; 対象患者): 前方循環(M2遠位, M3, ACAなど)の閉塞(=DMVO)による急性期脳梗塞患者 計286名
- E (Exposure; 介入): 血管内治療群 (156名)
- C (Comparator; 比較): 内科的治療群 (130名)
- O (Outcome; 転帰): 90日後の機能的転帰 (mRS 0-2: 機能的自立、mRS 0-1: 症状なし〜軽微)
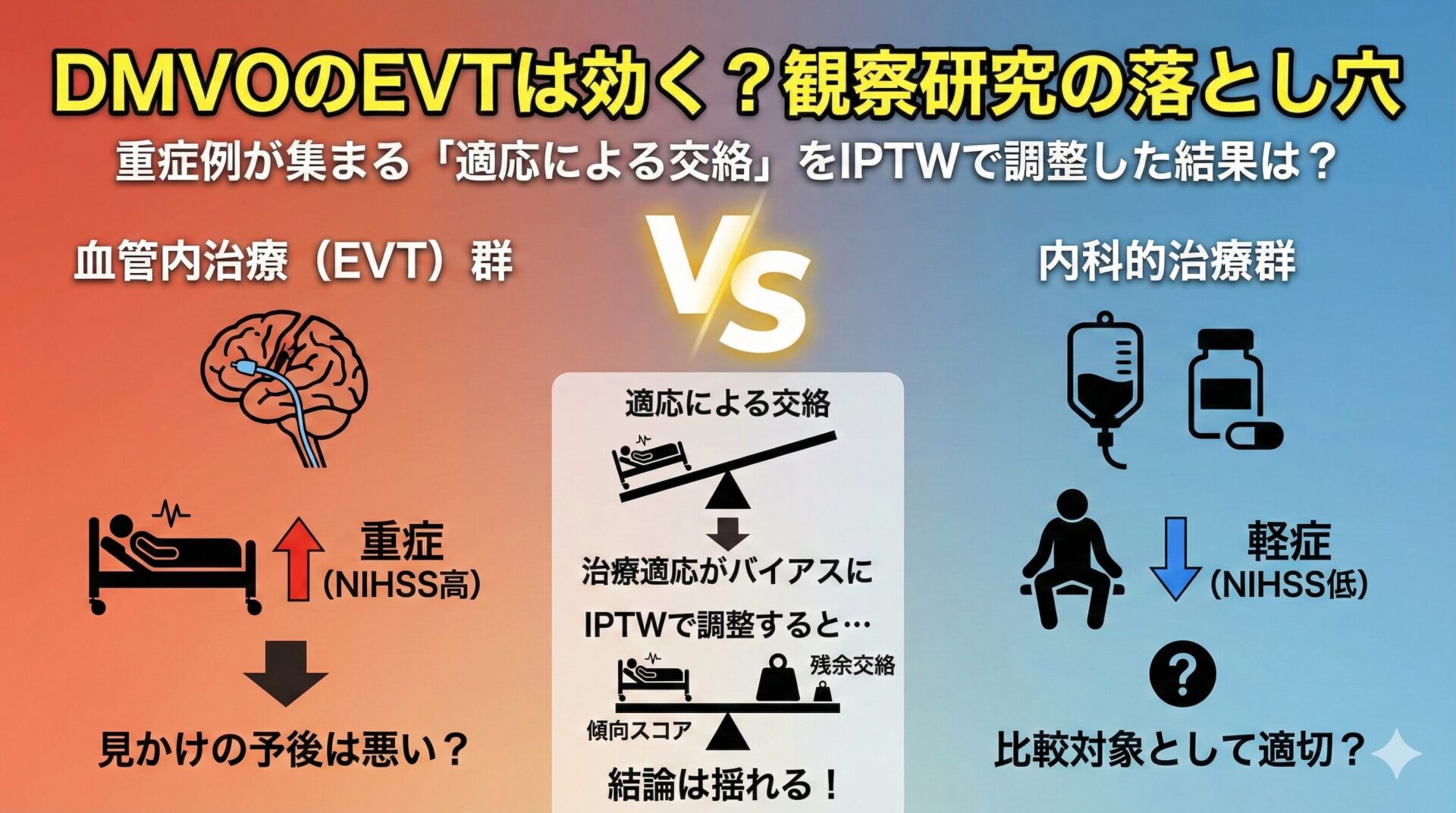
まず未調整:EVT群の方が重症に見える理由
この研究のTable 1(ベースラインの患者背景)を見て、治療の適応に注目してみましょう。最大のポイントは、脳卒中の重症度を示すNIHSSです。
- 血管内治療群: 入院時NIHSS中央値 13.5 (IQR 8.5–18.5)
- 内科的治療群: 入院時NIHSS中央値 7.0 (IQR 4–14)
この差は決定的です。
血管内治療群には、内科的治療群の約2倍も重症な患者が集積しています。
これはまさに臨床現場の意思決定を反映しています。
軽症であれば、まずは内科的治療で様子を見よう、となりやすい一方、
重症であれば、なんとかしなくてはと、より積極的な治療が適応と判断されやすいということを反映しています。
もし、この重症度の差を無視して2群を単純比較したら、どうなるでしょうか?
当然、元々重症なEVT群の見かけ上の予後は悪くなります。これが適応による交絡です。
逆確率重み付け(IPTW)とは何か?
この強力な交絡を統計的に調整するため、著者らは傾向スコアを用いた IPTW (Inverse Probability of Treatment Weighting; 逆確率重み付け) という手法を使っています。
これは、各患者の背景因子(年齢、NIHSSなど)から、血管内治療が選択される確率(=傾向スコア)を計算し、その確率の逆数で患者データに重みをつけ、あたかもランダム化比較試験を行ったかのように、両群の背景因子を揃えた、仮想的な集団を作り出す統計手法です。
この調整がうまくいったかを確認するツールが、論文の付録にあるLove Plotです。
調整前はバラバラだった両群の背景因子が、調整後はほぼ差がない状態に集まっていることが視覚的にわかります。
結果:
mRS 0–2は差なし、0–1はわずかに有利
安全性は同程度
では、IPTWで統計的に重症度の差を調整した後の結果はどうだったでしょうか。
- 90日後 mRS 0–2 (機能的自立):
- 調整後オッズ比 (aOR) 1.36 (95% CI, 0.84–2.19), p = 0.20
→ 有意差なし
- 調整後オッズ比 (aOR) 1.36 (95% CI, 0.84–2.19), p = 0.20
- 90日後 mRS 0–1 (症状なし〜軽微):
- 調整後オッズ比 (aOR) 1.71 (95% CI, 1.02–2.87), p = 0.04
→ 血管内治療群でわずかに良好
- 調整後オッズ比 (aOR) 1.71 (95% CI, 1.02–2.87), p = 0.04
- 安全性 (症候性頭蓋内出血, sICH):
- EVT群 4.0% vs MM群 3.1%, p = 0.90
→ 同程度
- EVT群 4.0% vs MM群 3.1%, p = 0.90
非常に観察研究らしい結果です。
mRS 0-2では有意差が出ませんでしたが、mRS 0-1ではわずかに血管内治療群に有利な結果となりました。
EVTは有効とも無効とも言い切れない、解釈が揺れる結果です。
DUSK研究との比較:なぜ結論が揺れるのか
この揺れる結果をどう解釈すべきでしょうか。
ここで補助線として、同じくDMVOに対する血管内治療と内科的治療の比較をIPTWで解析した、別の多施設観察研究、DUSK研究(Mohammaden M, et al. Stroke 2024) を見てみましょう。
- DUSK研究の結果: IPTWでの調整後、90日後のmRS(mRSシフト、mRS 0-2、mRS 0-1のいずれも)で、血管内治療群と内科的治療群に有意差は示されなかった。
Saber研究ではmRS 0-1は僅かに有利かも?でも、DUSK研究では差はなさそう。
このように、観察研究は研究の対象集団や調整方法によって結論が揺れることがよくあります。
なぜなら、IPTWは測定された因子(年齢、NIHSSなど)しか調整できないからです。
カルテ情報だけでは拾いきれない、医師の裁量(なんとなく重症感が強いなど)といった“未測定の交絡因子”までは調整できません。
このように、統計的調整後にもなお残ってしまう交絡を残余交絡と呼びます。
適応による交絡は特にこの残余交絡が残りやすく、非常に頑固なバイアスなのです。
どう読むか:target trialと今後のRCT
Saber研究やDUSK研究の結果をもって、DMVOに対する血管内治療は無効だと結論づけるのは早計です。
著者らが用いたIPTWは、観察データをできる限り理想的なランダム化試験(Target Trial; 目標試験)の条件に近づけようとする手法の一部です。
すなわち、もしこの患者集団で完全にランダム化したRCTを行ったとしたら?という問いを、観察研究の枠内で模倣しようとするアプローチです。
ただし、繰り返しになりますが、IPTWや傾向スコアを用いても、調整できるのはあくまで測定された交絡因子のみです。
臨床現場のこの患者はなんとなく重症そう、家族が強く希望した、といったデータ化されていない医師の判断や社会的要因までは調整できません。すなわち、観察研究ではどんなに精緻な解析を行っても、この残余交絡を完全に消し去ることはできません。
したがって、Target Trialの思考法を持ちながらも、観察研究の結果はあくまで仮説生成に位置づけ、最終的な結論は、交絡を原理的に排除できるランダム化比較試験 (RCT) の結果と一致するかどうかで確認する必要があります。
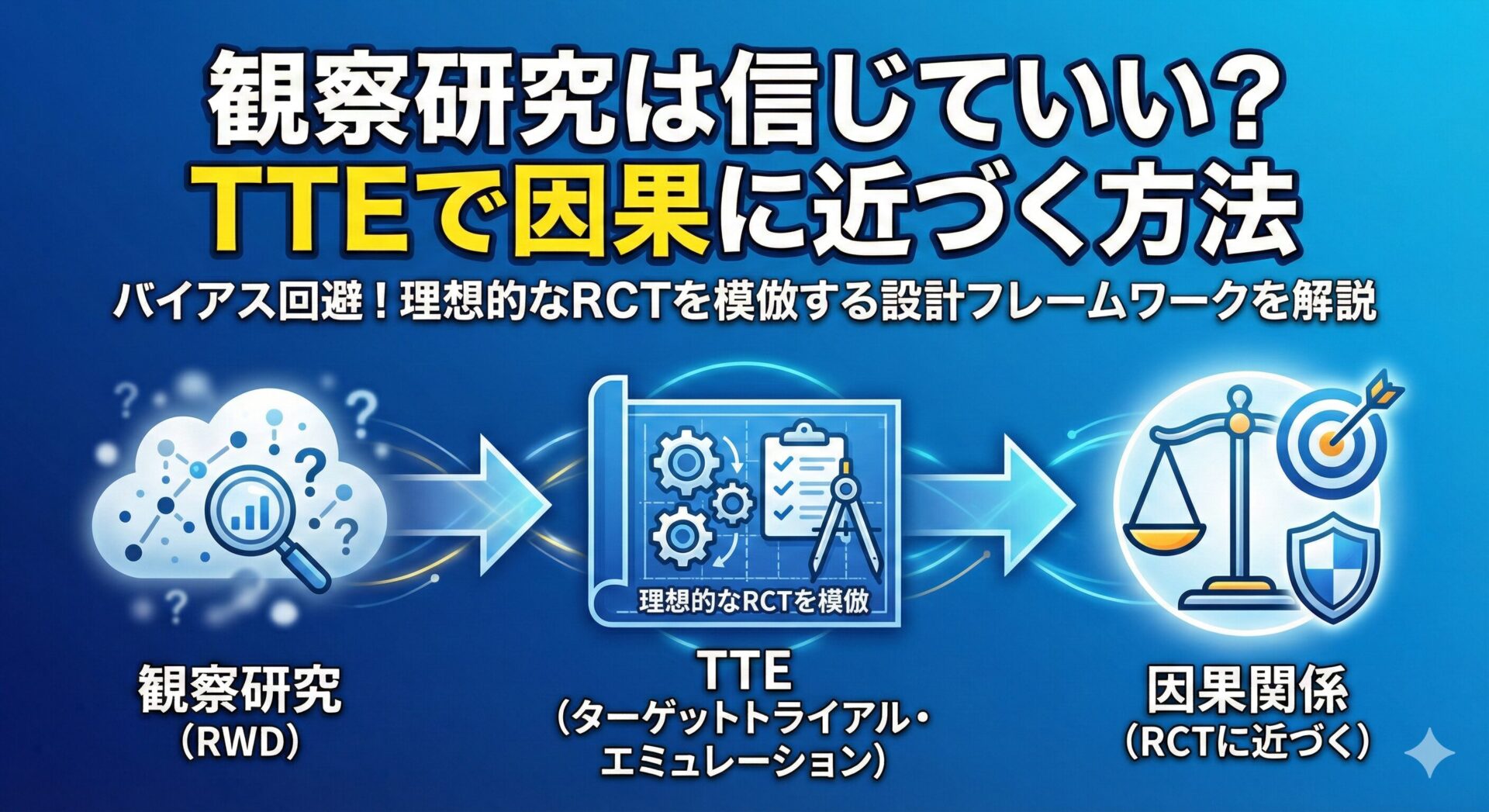
Target Trial Emulation(TTE)については、以下の記事で解説しているので、ご覧ください👇️
Take Home Message
- 観察研究で治療A vs 治療Bを読む際は、まず適応による交絡を疑い、両群のベースライン(特に重症度)を比較する。
- 重症例ほど使われる治療は、見かけ上効果がないあるいは有害に見えることがある。
- 傾向スコア(IPTWなど)による調整は強力だが万能ではない。
残余交絡の限界を常に意識する。 - 観察研究の結果は仮説生成と位置づけ、他の適切にデザインされた観察研究やRCTの結果と対比して解釈することが重要である。
よくある質問
Q1:適応による交絡はどう見抜く?
A1: まず、ベースラインの患者背景表(Table 1)で、重症度分布(本研究ではNIHSS)を確認します。治療群へ重症例が偏って集積していないかを見ます。さらに、IPTWなどが行われている場合、調整後のバランス(例:Love Plot)も併せて確認します。
Q2:この観察研究はEVT無効の証拠となる?
A2: いいえ。IPTW後、mRS 0–2は有意差なし、mRS 0–1はわずかに有利でした。これは効果がないことの証明ではありません。未測定の交絡(残余交絡)が結果に影響している可能性が否定できず、この研究の結論は仮説生成にとどまります。
Q3:他のエビデンスは?
A: DUSK研究(Stroke 2024)も同様の観察研究ですが、血管内治療と内科治療で有意差を示しませんでした。このように観察研究では結論が一致しないこともあり、コントラバシーな状況が続いています。最終的な結論は、現在進行中の複数のRCT(ランダム化比較試験)の結果によって示されることが期待されます。
参考文献
- Saber H, Desai SM, Haussen D, et al. Endovascular Therapy vs Medical Management for Patients With Acute Stroke With Medium Vessel Occlusion in the Anterior Circulation. JAMA Netw Open. 2022;5(10):e2238154.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/36279137/ - Nogueira RG, Doheim MF, Al-Bayati AR, et al. Distal Medium Vessel Occlusion Strokes: Understanding the Present and Paving the Way for a Better Future. J Stroke. 2024;26(2):190-202.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/38836268/ - Walker AM. Confounding by indication. Epidemiology. 1996;7(4):335-336.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/8793355/ - Sendor R, Stürmer T. Core concepts in pharmacoepidemiology: Confounding by indication and the role of active comparators. Pharmacoepidemiol Drug Saf. 2022;31(3):261-269.
PUBMED: https://pubmed.ncbi.nlm.nih.gov/35019190/